鋰電池廠家深度解讀鋰離子電池的電壓
鋰離子電池在充放電測試或者實際使用中,電壓參數主要包括平臺電壓、中值電壓、平均電壓、截止電壓等,典型放電曲線如圖1所示。
平臺電壓是指電壓變化最小而容量變化較大時對應的電壓值,磷酸鐵鋰、鈦酸鋰電池具有明顯的平臺電壓,在充放電曲線中可以明確確認電壓平臺。大部分電池的電壓平臺并不明顯,充放電測試時,通過電壓間隔采集數據,然后對電壓曲線做微分,通過dQ/dV的峰值確定平臺電壓。
中值電壓是電池容量一半時對應的電壓值,對于平臺比較明顯的材料,如磷酸鐵鋰和鈦酸鋰等,中值電壓一般就是平臺電壓。
平均電壓是電壓-容量曲線的有效面積(即電池充/放電能量)除以容量,計算公式為Ü = ∫U(t)*I(t)dt / ∫I(t)dt。在充放電測試數據中,充電或放電能量除以容量數據即為平均電壓。反過來,電池能量密度也是根據電池的平均電壓估算,即能量=容量*平均電壓/電池質量(或體積)。
截止電壓是是指電池放電時允許的最低電壓,電池充電時允許的最高電壓。如果電壓低于放電截止電壓后繼續放電,電池正極的電勢持續降低,而負極電勢會迅速上升,形成過度放電,過放電可能造成電極活性物質損傷,失去反應能力,使電池壽命縮短;還會導致負極銅箔分解并在正極析出,存在短路風險。如果充電電壓高于充電截止電壓,電池正極的電勢持續升高,造成正極材料過過度脫鋰,晶體結構破壞失效,電解液分解損耗鋰離子。而負極電勢會持續下降,過度嵌鋰,石墨層狀瓦解,極片表面析鋰等問題。
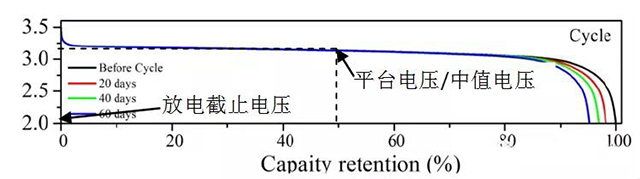
圖1 磷酸鐵鋰||石墨電池放電曲線
而實際上,電池的電壓U(電池)是由正極的電極電勢E(正極)和負極的電極電勢E(負極)之差確定的,由公式(1)所表示:
U(電池) = E(正極) - E(負極) 式(1)
在電池體系中,標準鋰電極普遍作為參考電極,正、負極材料的電極電勢一般都是反應物和產物與參比鋰電極之間反應而產生的電勢。如圖2所示,在充放電過程中,正負極材料脫鋰或嵌鋰,電極電勢發生變化,電池電壓就是兩者之差。
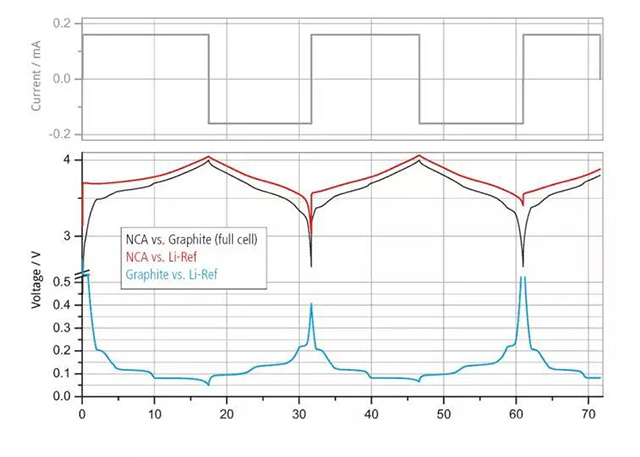
圖2 三電極電池電流、電壓曲線
因此,認識電池的電壓,首先要了解各種電極材料的電極電勢,了解材料的平衡電極電勢曲線能夠更好理解電池的電壓特性。
開路電壓是指電池在非工作狀態下即電路中無電流流過時,電池正負極之間的電勢差。將電極材料與金屬鋰組裝成紐扣半電池,開路電壓即電極材料的平衡電勢。
開路電壓測試方法
電極材料的平衡電勢測試過程為:電極材料制備成極片,與金屬鋰組裝成紐扣半電池,測得紐扣半電池在不同的SOC狀態下的開路電壓,并采用多項式或高斯擬合等確定開路電壓曲線的數學表達式。開路電壓測試方法主要包括:
(1)恒電流間歇滴定技術(galvanostatic intermittent titration technique,GITT), 基本原理是在某一特定環境下對測量體系施加一恒定電流并持續一段時間后切斷該電流,觀察施加電流段體系電位隨時間的變化以及弛豫后達到平衡的電壓(即開路電壓)。GITT測試舉例如下:(i)在C/50下充電直到電壓達到上限電壓,如4.2 V;(ii)靜置2小時;(iii)1C放電6min,記錄放電容量;(iv)靜置15min,記錄電壓;(v)重復步驟(iii)和(iv)共9次;(vi)在C/50下放電直到電壓達到下限電壓,如3.0V;(vii)將步驟(iii)和(iv)記錄的容量-電壓曲線,歸一化處理,做成SOC-電壓曲線,擬合得到開路電壓曲線的數學表達式。
(2)小電流充放電曲線,以特別低的倍率(如0.01C)電流恒流充放電,設置電壓上下限范圍,得到電池小電流充放電曲線,將電量一致的點作為曲線起點,對充放電曲線中的電壓取平均值,將曲線的橫坐標按照理論容量進行歸一化處理,然后利用曲線擬合得到開路電壓曲線。
電池極化
電流通過電極時,電極偏離平衡電極電勢的現象稱為電池的極化,極化產生過電勢。根據極化產生的原因可以將極化分為歐姆極化、濃差極化和電化學極化,如圖2所示。
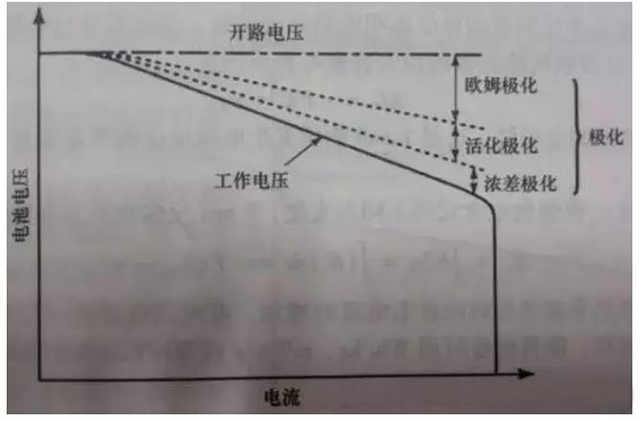
圖3 電流密度對極化的影響
(1)歐姆極化:由電池連接各部分的電阻造成,其壓降值遵循歐姆定律,電流減小,極化立即減小,電流停止后立即消失。
(2)電化學極化:由電極表面電化學反應的遲緩性造成極化。隨著電流變小,在微秒級內顯著降低。
(3)濃差極化:由于溶液中離子擴散過程的遲緩性,造成在一定電流下電極表面與溶液本體濃度差,產生極化。這種極化隨著電流下降,在宏觀的秒級(幾秒到幾十秒)上降低或消失。
電池的內阻隨電池放電電流的增大而增大,這主要是由于大的放電電流使得電池的極化趨勢增大,并且放電電流越大,則極化的趨勢就越明顯,如圖2所示。根據歐姆定律:V=E0-I×RT,內部整體電阻RT的增加,則電池電壓達到放電截止電壓所需要的時間也相應減少,故放出的容量也減少。
鋰離子電池實質上是一種鋰離子濃差電池,鋰離子電池的充放電過程為鋰離子在正負極的嵌入、脫出的過程。影響鋰離子電池極化的因素包括:
(1)電解液的影響:電解液電導率低是鋰離子電池極化發生的主要原因。在一般溫度范圍內,鋰離子電池用電解液的電導率一般只有0.01~0.1S/cm,,是水溶液的百分之一。因此,鋰離子電池在大電流放電時,來不及從電解液中補充Li+,會發生極化現象。提高電解液的導電能力是改善鋰離子電池大電流放電能力的關鍵因素。
(2)正負極材料的影響:正負極材料顆粒大鋰離子擴散到表面的通道加長,不利于大倍率放電。
(3)導電劑:導電劑的含量是影響高倍率放電性能的重要因素。如果正極配方中的導電劑含量不足,大電流放電時電子不能及時地轉移,極化內阻迅速增大,使電池的電壓很快降低到放電截止電壓。
(4)極片設計的影響:
極片厚度:大電流放電的情況下,活性物質反應速度很快,要求鋰離子能在材料中迅速的嵌入、脫出,若是極片較厚,鋰離子擴散的路徑增加,極片厚度方向會產生很大的鋰離子濃度梯度。
壓實密度:極片的壓實密度較大,孔隙變得更小,則極片厚度方向鋰離子運動的路徑更長。另外,壓實密度過大,材料與電解液之間接觸面積減小,電極反應場所減少,電池內阻也會增大。
(5)SEI膜的影響:SEI 膜的形成增加了電極/電解液界面的電阻,造成電壓滯后即極化。
電池的工作電壓
工作電壓又稱端電壓,是指電池在工作狀態下即電路中有電流流過時電池正負極之間的電勢差。在電池放電工作狀態下,當電流流過電池內部時,需克服電池的內阻所造成阻力,會造成歐姆壓降和電極極化,故工作電壓總是低于開路電壓,充電時則與之相反,端電壓總是高于開路電壓。即極化的結果使電池放電時端電壓低于電池的電動勢,電池充電時,電池的端電壓高于電池的電動勢。
由于極化現象的存在,會導致電池在充放電過程中瞬時電壓與實際電壓會產生一定的偏差。充電時,瞬時電壓略高于實際電壓,充電結束后極化消失,電壓回落;放電時,瞬時電壓略低于實際電壓,放電結束后極化消失,電壓回升。
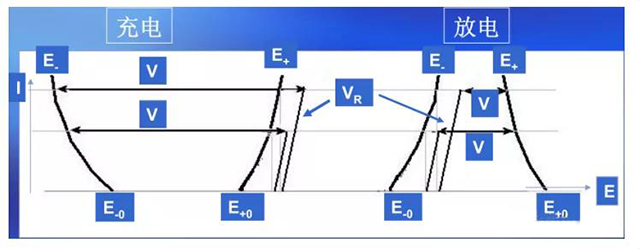
圖4 電池電壓的組成及其與工作電流的關系
綜合以上所述,電池端電壓的組成如圖3所示,表達式為:
充電:VCH = (E+ - E-)+ VR =(E+0+η+)- (E-0 - η-)+ VR
放電:VD = (E+ - E-)- VR =(E+0-η+)- (E-0 + η-)- VR
為什么有些材料具有明顯的電壓平臺而有些沒有?
熱力學中,自由度 F 是當系統為平衡狀態時,在不改變相態的數量情況下,可獨立改變的因素(如溫度和壓力),這些變量的數目叫做自由度數。系統的自由度跟其他變量的關系:
F = C - P + n
其中 F:表示系統的自由度;C :系統的獨立組元數;P :相態數目;n :外界因素,多數取n=2,代表壓力和溫度。
針對鋰離子電化學體系,外界因素n=2,分別取電壓和溫度。假定鋰離子電極材料在充放電過程中溫度和壓力恒定不變。在此,我們討論二元系(C=2),如果在一個粒子中含有一個相,即P=1,則F=1,化學勢是一個自由度,隨鋰濃度的變化而變化(例如固溶體鈷酸鋰,一個相,鋰濃度不斷變化)。
如果粒子中包含兩個相,即P=2,則F=0。當兩相共存時,在一個二元系電極材料中存在平坦的電壓平臺(例如磷酸鐵鋰,兩相共存,每個相中鋰濃度是不變的)。
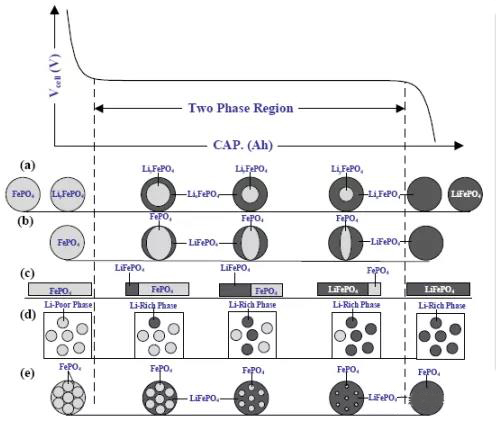
圖5 LFP材料電壓曲線及相變過程示意圖
本文鏈接:http://m.qhgfjy.com.cn{dede:field.arcurl/}
諾信新聞,諾信公司新聞,鋰電池行業新聞,展會新聞